-
取向力 编辑
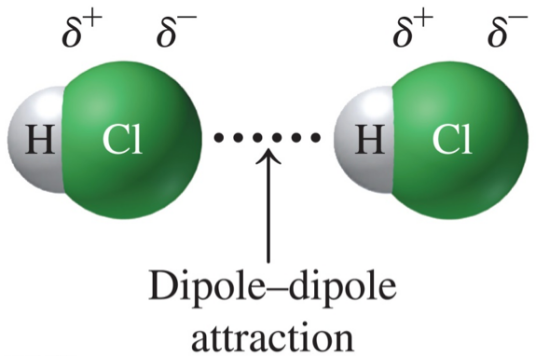
取向力(dipole-dipole attraction)又称定向力,是极性分子与极性分子之间的固有偶极与固有偶极之间的静电引力称为取向力,又叫定向力。因为两个极性分子相互接近时,同极相斥,异极相吸,使分子发生相对转动,极性分子按一定方向排列,并由静电引力互相吸引。当分子之间接近到一定距离后,排斥和吸引达到相对平衡,从而使体系能量达到最小值。极性分子固有偶极间存在作用力是葛生(Keeson)于1912年首先提出来的,因此取向力也称为葛生力。取向力的本质是静电引力,取向力与分子偶极矩的平方成正比,与热力学温度成反比,与分子间距离的3次方成反比。
中文名:取向力
外文名:dipole-dipole attraction, dipole-dipole force
本质:静电引力
相关学科:物理、化学
取向力只有极性分子与极性分子之间才存在。取向力的本质是静电引力,其大小决定于极性分子的偶极矩。分子的极性越强,偶极矩越大,取向力越大。如:HI 、HBr 、HCl 的偶极矩依次增大,因而其取向力依次增大。此外,取向力还受温度的影响,温度越高,取向力越弱。
对大多数极性分子,取向力仅占其范德华力构成中的很小分额,只有少数强极性分子例外。
分子相互接近时,极性分子 的永久偶极间同极相斥、异极相吸,
— 个分子的带负电的一端和另一个分子带正电的一端接近,使极
性分子按一定方向排列。这种由 于取向而在极性分子的永久偶极间
产生的静电作用力称为取向力。
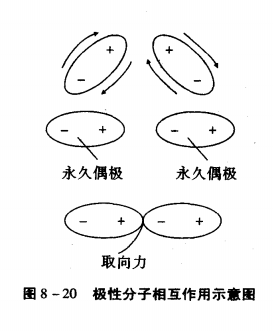 极性分子相互作用示意图
极性分子相互作用示意图
(1)分子的偶极矩越大,取向力就越大;如:HI 、HBr 、HCl 的偶极矩依次增大,因而其取向力依次增大。
(2)分子间的距离越大,取向力将减弱。
(3)此外,当温度升高时,取向力会减少。因为温度升高时,分子的热运动加剧,破坏了分子的有序排列,减少了取向的趋势。
极性分子与极性分子之间,取向力、诱导力、色散力都存在;极性分子与非极性分子之间,则存在诱导力和色散力;非极性分子与非极性分子之间,则只存在色散力。这三种类型的力的比例大小,决定于相互作用分子的极性和变形性。极性越大,取向力的作用越重要;变形性越大,色散力就越重要;诱导力则与这两种因素都有关。但对大多数分子来说,色散力是主要的。实验证明,对大多数分子来说,色散力是主要的;只有偶极矩很大的分子(如水),取向力才是主要的;而诱导力通常是很小的。极化率α反映分子中的电子云是否容易变形。虽然范德华力只有0.4—4.0kJ/mol,但是在大量大分子间的相互作用则会变得十分稳固。比如C—H 在苯中范德华力有7 kJ/mol,而在溶菌酶和糖结合底物范德华力却有60kJ/mol,范德华力具有加和性。
1、本站所有文本、信息、视频文件等,仅代表本站观点或作者本人观点,请网友谨慎参考使用。
2、本站信息均为作者提供和网友推荐收集整理而来,仅供学习和研究使用。
3、对任何由于使用本站内容而引起的诉讼、纠纷,本站不承担任何责任。
4、如有侵犯你版权的,请来信(邮箱:baike52199@gmail.com)指出,核实后,本站将立即删除。