-
沉淀 编辑
从字意上理解,沉淀是指有一种物质由于密度比它所在的体系大且又不溶于它们从而沉了下去。沉淀(precipitation)操作则是将溶液中的目的产物或主要杂质以无定形固相形式析出再进行分离的单元操作。 沉淀法有等电点沉淀法、盐析法、有机溶剂沉淀法等。
定义
从字意上理解就是指有一种物质由于密度比它所在的溶剂或溶液大且又不溶于它们从而沉了下去。
事实上沉淀多为难溶物(20°C时每100克水中溶解的克数小于0.01克)。
原理
从液相中产生一个可分离的固相的过程,或是从过饱和溶液中析出的难溶物质。沉淀作用表示一个新的凝结相的形成过程,或由于加入沉淀剂使某些离子成为难溶化合物而沉积的过程。产生沉淀的化学反应称为沉淀反应。物质的沉淀和溶解是一个平衡过程,通常用溶度积常数Ksp来判断难溶盐是沉淀还是溶解。溶度积常数是指在一定温度下,在难溶电解质的饱和溶液中,组成沉淀的各离子浓度的乘积为一常数。分析化学中经常利用这一关系,借加入同离子而使沉淀溶解度降低,使残留在溶液中的被测组分小到可以忽略的程度。
分类
沉淀可分为晶形沉淀和非晶形沉淀两大类型。硫酸钡是典型的晶形沉淀,Fe2O3·nH2O是典型的非晶形沉淀。晶形沉淀内部排列较规则,结构紧密,颗粒较大,易于沉降和过滤;非晶形沉淀颗粒很小,没有明显的晶格,排列杂乱,结构疏松,体积庞大,易吸附杂质,难以过滤,也难以洗干净。
制取
实验证明,沉淀类型和颗粒大小,既取决于物质的本性,又取决于沉淀的条件。在实际工作中,须根据不同的沉淀类型选择不同的沉淀条件,以获得合乎要求的沉淀。对晶形沉淀,要在热的稀溶液中,在搅拌下慢慢加入稀沉淀剂进行沉淀。沉淀以后,将沉淀与母液一起放置,使其“陈化”,以使不完整的晶粒转化变得较完整,小晶粒转化为大晶粒。而对非晶形沉淀,则在热的浓溶液中进行沉淀,同时加入大量电解质以加速沉淀微粒凝聚,防止形成胶体溶液。沉淀完毕,立即过滤,不必陈化。
作用
在经典的定性分析中,几乎一半以上的检出反应是沉淀反应。在定量分析中,它是重量法和沉淀滴定法的基础。沉淀反应也是常用的分离方法,既可将欲测组分分离出来,也可将其它共存的干扰组分沉淀除去。
种类
 氯化银沉淀
氯化银沉淀
Cu(OH)2蓝色絮状沉淀
BaSO4白色沉淀
Mg(OH)2白色沉淀
Al(OH)3白色沉淀
BaCO3白色沉淀
CuO黑色沉淀
Cu2O红色沉淀
Cu2(OH)2CO3暗绿色沉淀
CaCO3白色沉淀
Fe(OH)3红褐色沉淀
Fe(OH)2为白色絮状沉淀(在空气中很快变成灰绿色,再变成Fe(OH)3红褐色沉淀)
Fe2O3 红棕色沉淀
FeO 黑色沉淀
FeCO3 灰色沉淀
FeS2 黄色沉淀
AgBr淡黄色沉淀
Ag2CO3 黄色沉淀
AgBr 浅黄色沉淀
AgCl 白色沉淀
Ag3PO4黄色沉淀
PbS黑色沉淀
条件
金属离子 | pH值 | |
开始沉淀 | 完全沉淀 | |
Fe3+ | 2.7 | 3.7 |
Al3+ | 3.7 | 4.7 |
Cu2+ | 4.4 | 6.4 |
Zn2+ | 6 | 8 |
Co2+ | 6.7 | 8.7 |
Fe2+ | 7.6 | 9.6 |
Mn2+ | 7.8 | 9.8 |
Mg2+ | 9.3 | 10.8 |
Ca(OH)2+CO2 = CaCO3↓+ H2O澄清石灰水变浑浊 应用CO2检验和石灰浆粉刷墙壁
Ca(HCO3)2 = CaCO3↓+H2O+CO2↑ 白色沉淀、产生使澄清石灰水变浑浊的气体水垢形成。钟乳石、石笋的形成
HCl+AgNO3 = AgCl↓+HNO3 生成白色沉淀、不溶解于稀硝酸检验Cl-的原理
Ba(OH)2+ H2SO4 = BaSO4↓+2H2O 生成白色沉淀、不溶解于稀硝酸检验SO42-的原理
BaCl2+ H2SO4 = BaSO4↓+2HCl 生成白色沉淀、不溶解于稀硝酸检验SO42-的原理
Ba(NO3)2+H2SO4 = BaSO4↓+2HNO3 生成白色沉淀、不溶解于稀硝酸检验SO42-的原理
FeCl3+3NaOH = Fe(OH)3↓+3NaCl 溶液黄色褪去、有红褐色沉淀生成
AlCl3+3NaOH = Al(OH)3↓+3NaCl 有白色沉淀生成
MgCl2+2NaOH = Mg(OH)2↓+2NaCl有白色沉淀产生
CuCl2+2NaOH = Cu(OH)2↓+2NaCl 溶液蓝色褪去、有蓝色沉淀生成
CaO+ H2O = Ca(OH)2 白色块状固体变为粉末、生石灰制备石灰浆
Ca(OH)2+SO2 = CaSO3↓+ H2O 有白色沉淀生成 初中一般不用
Ca(OH)2+Na2CO3 = CaCO3↓+2NaOH 有白色沉淀生成 工业制取烧碱、实验室制少量烧碱
Ba(OH)2+Na2CO3 = BaCO3↓+2NaOH 有白色沉淀生成
Ca(OH)2+K2CO3 = CaCO3↓ +2KOH 有白色沉淀生成
AgNO3+NaCl = AgCl↓+NaNO3 白色不溶解于稀硝酸的沉淀(其他氯化物类似反应) 应用于检验溶液中的氯离子
BaCl2 + Na2SO4 = BaSO4↓+2NaCl 白色不溶解于稀硝酸的沉淀(其他硫酸盐类似反应) 应用于检验硫酸根离子
CaCl2+Na2CO3 = CaCO3↓+2NaCl 有白色沉淀生成
MgCl2+Ba(OH)2 = BaCl2+Mg(OH)2↓ 有白色沉淀生成
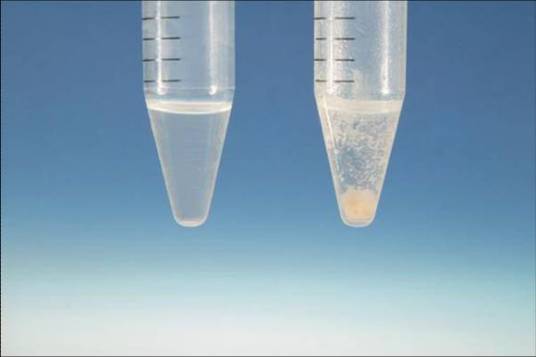
 饮料瓶中的沉淀物
饮料瓶中的沉淀物
2.絮凝沉淀。悬浮颗粒的浓度比较高(50~500mg/L),在沉淀过程中能发生凝聚或絮凝作用,使悬浮颗粒互相碰撞凝结,颗粒质量逐渐增加,沉降速度逐渐加快。经过混凝处理的水中颗粒的沉淀、初沉池后期、生物膜法二沉池、活性污泥法二沉池初期等均属絮凝沉淀。
3.拥挤沉淀。悬浮颗粒的浓度很高(大于500mg/L),在沉降过程中,产生颗粒互相干扰的现象,在清水与浑水之间形成明显的交界面(混液面),并逐渐向下移动,因此又称成层沉淀。活性污泥法二沉池的后期、浓缩池上部等均属这种沉淀类型。
4.压缩沉淀。悬浮颗粒浓度特高(以至于不再称水中颗粒物浓度,而称固体中的含水率),在沉降过程中,颗粒相互接触,靠重力压缩下层颗粒,使下层颗粒间隙中的液体被挤出界面上流,固体颗粒群被浓缩。活性污泥法二沉池污泥斗中、浓缩池中污泥的浓缩过程属此类型。
滤过是使沉淀和母液分开,与过量沉淀剂、共存组分或其他杂质分离,从而得到纯净的沉淀。
若后续处理需要灼烧的沉淀,用定量滤纸过滤,这种滤纸已用HCl和HF处理,大部分无机物已被除去,每张滤纸灼烧后残留灰分小于0.2mg。根据沉淀的性质,选择疏密程度不同的定量滤纸。①一般无定形沉淀,应选用疏松的快速滤纸;②粗粒的晶形沉淀,可选用较紧密的中速滤纸;③较细粒的晶形沉淀,应选用最紧密的慢速滤纸。若只需烘干即可得到称量形式的沉淀,常用玻璃砂芯坩埚或玻璃砂芯漏斗减压抽滤,根据沉淀的性状选择不同型号滤器。
过滤时均采用“倾泻法”。若沉淀的溶解度随温度变化不大,采用趁热过滤更好。
(二)沉淀的洗涤
沉淀的洗涤是为了洗去沉淀表面吸附的杂质和混杂在沉淀中的母液。洗涤时选择合适的洗液,可减少沉淀的溶解损失和避免形成胶体。选择洗液的原则是:①溶解度小而不易形成胶体的沉淀可采用蒸馏水洗涤;②溶解度大的晶形沉淀可用稀沉淀剂(干燥或灼烧可除去)溶液或沉淀的饱和溶液洗涤;③对于易胶溶的无定形沉淀,应选用易挥发的电解质稀溶液洗涤;④沉淀的溶解度随温度变化不大时,可用热溶液洗涤。采用倾泻法洗涤沉淀,洗涤过程遵循少量多次原则,洗涤干净与否可采用特效反应进行检查。
(三)沉淀的干燥或灼烧和恒重
为了除去沉淀中的水分和挥发性物质,以及使沉淀分解为组分恒定的称量形式,沉淀需要干燥或灼烧。干燥是在110~120℃烘40~60分钟,除去沉淀中的水分和挥发性物质得到沉淀的称量形式。灼烧是在800℃以上,彻底去除水分和挥发性物质,并使沉淀分解为组成恒定的称量形式。
1、本站所有文本、信息、视频文件等,仅代表本站观点或作者本人观点,请网友谨慎参考使用。
2、本站信息均为作者提供和网友推荐收集整理而来,仅供学习和研究使用。
3、对任何由于使用本站内容而引起的诉讼、纠纷,本站不承担任何责任。
4、如有侵犯你版权的,请来信(邮箱:baike52199@gmail.com)指出,核实后,本站将立即删除。