-
元素周期表 编辑
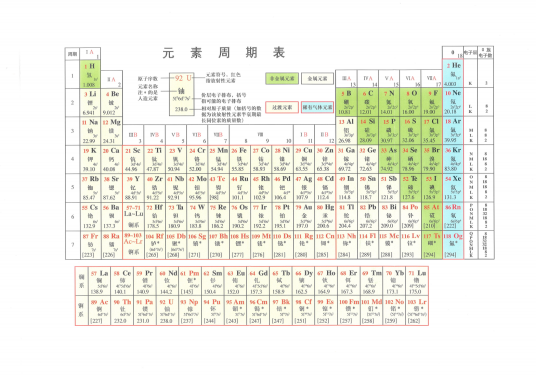
化学元素周期表(Periodic table of elements)是根据元素原子核电荷数从小至大排序的化学元素列表。列表大体呈长方形,某些元素周期中留有空格,使特性相近的元素归在同一族中,如碱金属元素、碱土金属、卤族元素、稀有气体,非金属,过渡元素等。这使周期表中形成元素分区且分有七主族、七副族、Ⅷ族、18族。由于周期表能够准确地预测各种元素的特性及其之间的关系,因此它在化学及其他科学范畴中被广泛使用,作为分析化学行为时十分有用的框架。俄国化学家德米特里·伊万诺维奇·门捷列夫(Dmitri Mendeleev)于1869年总结发表此周期表(第一代元素周期表),此后不断有人提出各种类型周期表不下170余种,归纳起来主要有:短式表(以门捷列夫为代表)、长式表(以维尔纳式为代表)、特长表(以波尔塔式为代表);平面螺线表和圆形表(以达姆开夫式为代表);立体周期表(以莱西的圆锥柱立体表为代表)等众多类型表。注:中国教学上长期使用的是长式周期表,即维尔纳式为代表。
中文名:元素周期表
外文名:periodic table of elements
别名:元素表
所属学科:化学
创造者:德米特里·伊万诺维奇·门捷列夫
概念:化学元素周期列表
发表时间:1869年
元素分区:七主族、七副族、Ⅷ族、18族
 德米特里·伊万诺维奇·门捷列夫
德米特里·伊万诺维奇·门捷列夫
在周期表中,元素是以元素的原子序数排列,最小的排行最先。表中一横行称为一个周期,一列称为一个族。 原子半径由左到右依次减小,上到下依次增大。
在化学教科书和字典中,都附有一张“元素周期表(英文:the periodic table of elements)”。这张表揭示了物质世界的秘密,把一些看来似乎互不相关的元素统一起来,组成了一个完整的自然体系。它的发明,是近代化学史上的一个创举,对于促进化学的发展,起了巨大的作用。看到这张表,人们便会想到它的最早发明者——门捷列夫。1869年,俄国化学家门捷列夫按照相对原子质量由小到大排列,将化学性质相似的元素放在同一纵行,编制出第一张元素周期表。元素周期表揭示了化学元素之间的内在联系,使其构成了一个完整的体系,成为化学发展史上的重要里程碑之一。随着科学的发展,元素周期表中未知元素留下的空位先后被填满。当原子结构的奥秘被发现时,编排依据由相对原子质量改为原子的质子数(核外电子数或核电荷数),形成现行的元素周期表。
按照元素在周期表中的顺序给元素编号,得到原子序数。原子序数跟元素的原子结构有如下关系:
质子数=原子序数=核外电子数=核电荷数
利用周期表,门捷列夫成功的预测当时尚未发现的元素的特性(镓、钪、锗)。1913年英国科学家莫色勒利用阴极射线撞击金属产生射线X,发现原子序数越大,X射线的频率就越高,因此他认为核的正电荷决定了元素的化学性质,并把元素依照核内正电荷(即质子数或原子序数)排列。后来又经过多名科学家多年的修订才形成当代的周期表。将元素按照相对原子质量由小到大依次排列,并将化学性质相似的元素放在一个纵列。每一种元素都有一个序号,大小恰好等于该元素原子的核内质子数,这个序号称为原子序数。在周期表中,元素是以元素的原子序数排列,最小的排行最前。表中一横行称为一个周期,一列称为一个族。
原子的核外电子排布和性质有明显的规律性,科学家们是按原子序数递增排列,将电子层数相同的元素放在同一行,将最外层电子数相同的元素放在同一列。
元素周期表有7个周期,18个族。每一个横行叫作一个周期,每一个纵行叫作一个族(VIII族包含三个纵列)。这7个周期又可分成短周期(1、2、3)、长周期(4、5、6、7)。共有18个族,从左到右每个纵列算一族。例如:氢属于1族元素,而氦属于0族元素。
元素在周期表中的位置不仅反映了元素的原子结构,也显示了元素性质的递变规律和元素之间的内在联系。使其构成了一个完整的体系,被称为化学发展的重要里程碑之一。
同一周期内,从左到右,元素核外电子层数相同,最外层电子数依次递增,原子半径递减(18族元素除外)。失电子能力逐渐减弱,获电子能力逐渐增强,金属性逐渐减弱,非金属性逐渐增强。元素的最高正氧化数从左到右递增(没有正价的除外),最低负氧化数从左到右递增(第一周期除外,第二周期的O、F元素除外)。
同一族中,由上而下,最外层电子数相同,核外电子层数逐渐增多,原子半径增大,原子序数递增,元素金属性递增,非金属性递减。
元素周期表的意义重大,科学家正是用此来寻找新型元素及化合物。
2015年12月31日美国《科学新闻》双周刊网站发表了题为《四种元素在元素周期表上获得永久席位》的报道。国际纯粹与应用化学联合会(IUPAC)宣布俄罗斯和美国的研究团队已获得充分的证据,证明其发现了115、117和118号元素。此外,该联合会已认可日本理化学研究所的科研人员发现了113号元素。两个研究团队通过让质量较轻的核子相互撞击,并跟踪其后产生的放射性超重元素的衰变情况,合成了上述四种元素。IUPAC执行理事林恩·瑟比说,有关确认新元素的报告将于2016年初公布。官方对这些元素的认可意味着它们的发现者有权为其命名并设计符号。113号元素将成为首个由亚洲人发现并命名的元素,于2016年6月正式命名为Nihonium,符号Nh。
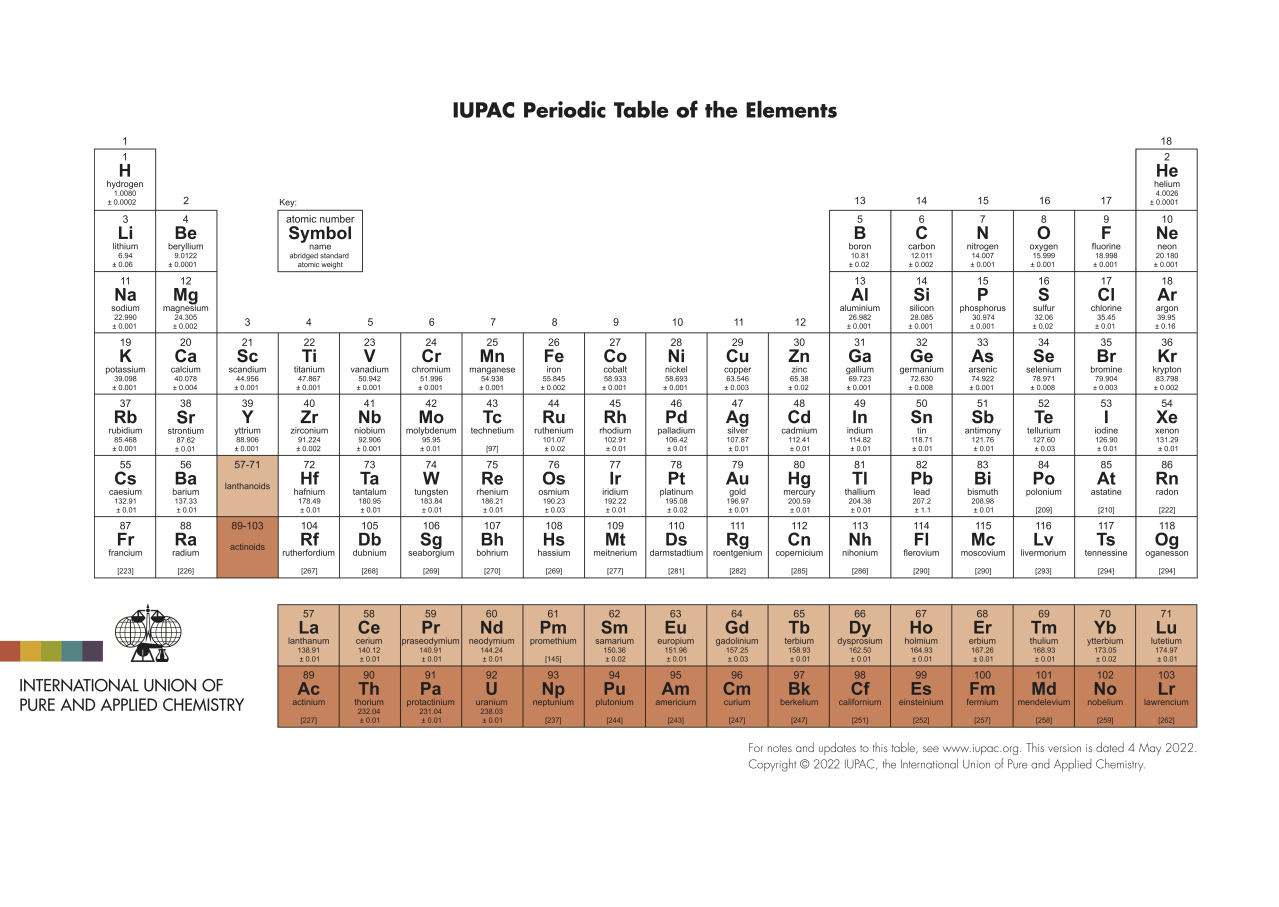 IUPAC元素周期表 2022.05.04
IUPAC元素周期表 2022.05.04
2015年12月30日,国际纯粹与应用化学联合会宣布第113、115、117、118号元素存在,它们将由日本、俄罗斯和美国科学家命名。IUPAC官方宣布,元素周期表已经加入4个新元素。
2016年6月8日,国际纯粹与应用化学联合会宣布,将合成化学元素第113号(Nh)、115号(Mc)、117号(Ts)和118号(Og)提名为化学新元素。
2017年5月9日,中国科学院、国家语言文字工作委员会、全国科学技术名词审定委员会在北京联合举行新闻发布会,正式向社会发布113号元素、115号元素、117号元素、118号元素中文名称,分别为“鿭”、“镆”、“鿬”、“鿫”。
分区名称 | 详细介绍 |
|---|---|
s区元素 | 周期表中第1列和第2列为s区元素,他们的价电子构型分别为ns1和ns2。其中第1列包括氢(H)和碱金属锂(Li)、钠(Na)、钾(K)、铷(Rb)、铯(Cs)、钫(Fr),即第1主族(IA)。第2列包括碱土金属铍(Be)、镁(Mg)、钙(Ca)、锶(Sr)、钡(Ba)、镭(Ra),即第2主族(IIA)。这两族元素位于元素周期表左侧,它们在化学反应中参与成键的只是s电子,所以化学性质比较简单,最为突出的是其氧化物和氢氧化物的碱性,因而得名。 |
p区元素 | 周期表里的第13~18列,即III A~VIIA和零族,共6族、31种元素为p区元素。它们的价电子构型为ns2np1~6。在B、Si、As、Te下划线,可将这个区域一分为二,右上方为非金属区,左下方为金属区。21种非金属元素位于右上方,其中在常温常压下,单质为气态的共10种,其名字都有“气”字头;单质为液态的只有一种,就是溴,它的名字有“氵”旁;其他10种非金属在常温常压下为固态,都是“石”为旁。左下方的金属元素都有“钅”字旁。在斜角线两侧的元素如B、Si、Ge、As、Sb、Te等既有金属性也有非金属性,有半金属之称,是制造半导体材料的重要元素。p区元素最重的性质是氧化还原性和酸碱性。 |
d区元素 | d区元素是指周期表中第3~12,即IIIB、IVB、VB、VIB、VIIB、VIII、IB和IIB族的元素,共有30种金属元素,其价电子构型为(n-1)d1~10ns1~2,因为位于典型的金属元素(s区元素)与典型的非金属元素(p区元素)之间,d区元素和f区元素又共称为过渡元素或过渡金属。d区第四周期被称为第一过渡系,第五和第六周期分别为第二过度系和第三过度系。d区元素各族元素性质的差异源于次外层d电子的不同,所以和主族元素相比,各族之间的差别较小。 第11列的IB族的铜(Cu)、银(Ag)、金(Au)和第12列的IIB族的锌(Zn)、镉(Cd)、汞(Hg)最外层有ns1~2价电子,容易形成+1或+2价化合物,在认识周期律的初期认为它们与元素IA族和IIA族相似,所以将它们标记为IB副族和IIB副族,如今可知其次外层为18电子结构,与s区次外层为8电子结构不同,故归于d区或另立ds区都可以。 |
f区元素 | f区元素由镧系元素和锕系元素组成,共30种元素,位于元素周期表下方,多数具有f电子。其中,15种镧系元素以及IIIB族的钪(Sc)、钇(Y)共计17种元素又被称为稀土元素。 |
注*的是人造元素 | ||||||||||||||||||
周期 | ⅠA | ⅡA | ⅢB | ⅣB | ⅤB | ⅥB | ⅦB | Ⅷ | ⅠB | ⅡB | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 18 | ||
1 | H 氢 | - | He 氦 | |||||||||||||||
2 | Li 锂 | Be 铍 | - | B 硼 | C 碳 | N 氮 | O 氧 | F 氟 | Ne 氖 | |||||||||
3 | Na 钠 | Mg 镁 | Al 铝 | Si 硅 | P 磷 | S 硫 | Cl 氯 | Ar 氩 | ||||||||||
4 | K 钾 | Ca 钙 | Sc 钪 | Ti 钛 | V 钒 | Cr 铬 | Mn 锰 | Fe 铁 | Co 钴 | Ni 镍 | Cu 铜 | Zn 锌 | Ga 镓 | Ge 锗 | As 砷 | Se 硒 | Br 溴 | Kr 氪 |
5 | Rb 铷 | Sr 锶 | Y 钇 | Zr 锆 | Nb 铌 | Mo 钼 | Tc 锝 | Ru 钌 | Rh 铑 | Pd 钯 | Ag 银 | Cd 镉 | In 铟 | Sn 锡 | Sb 锑 | Te 碲 | I 碘 | Xe 氙 |
6 | Cs 铯 | Ba 钡 | La-Lu 镧系 | Hf 铪 | Ta 钽 | W 钨 | Re 铼 | Os 锇 | Ir 铱 | Pt 铂 | Au 金 | Hg 汞 | Tl 铊 | Pb 铅 | Bi 铋 | Po 钋 | At 砹 | Rn 氡 |
7 | Fr 钫 | Ra 镭 | Ac-Lr 锕系 | Rf
1、本站所有文本、信息、视频文件等,仅代表本站观点或作者本人观点,请网友谨慎参考使用。 词条信息
| ||||||||||||||